Alzheimer-Fibrillen atomar aufgelöst
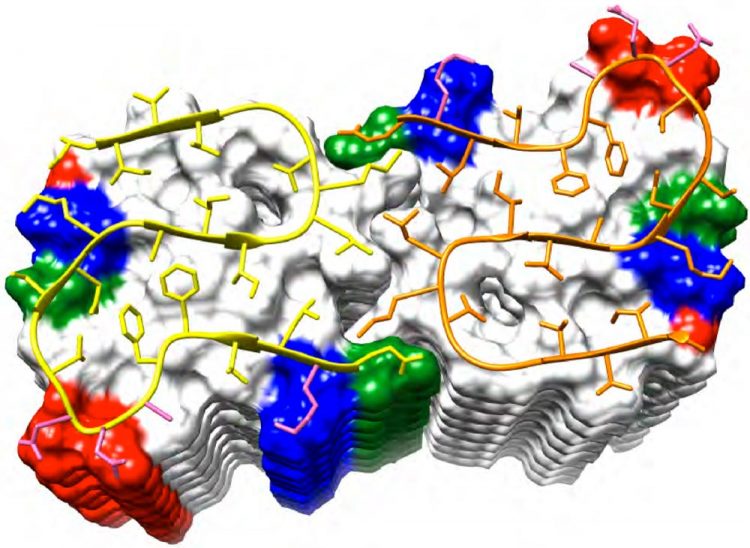
Struktur der Amyloid-Beta 1–42 Fibrille
Weltweit sind mindestens 60 Prozent der Demenzerkrankungen auf die Alzheimer-Krankheit zurückzuführen. Sie verursacht enormes menschliches Leid und bringt hohe Kosten mit sich. Heilung oder eine ursächliche Therapie gibt es bis heute nicht. Unter anderem deshalb, weil der genaue Ablauf der Krankheit auf molekularer Ebene im Gehirn noch viele Rätsel aufgibt.
Bekannt ist, dass das Beta-Amyloid-Protein eine entscheidende Rolle spielt. Es handelt sich um ein 39 bis 42 Aminosäuren langes, für Nervenzellen giftiges Peptid, das langgestreckte Fibrillen (Fasern) bilden kann. Beta-Amyloid-Peptid 1–42 und Beta-Amyloid-Peptid 1-40 sind die beiden Hauptformen, die in senilen Plaques vorkommen. Warum diese zum Untergang von Nervenzellen im Gehirn führen, ist nicht bekannt, aber von größtem Interesse für die Entwicklung von Alzheimer-Arzneimitteln.
In einer Zusammenarbeit zwischen der ETH Zürich, der Université de Lyon und der Goethe-Universität Frankfurt am Main sowie Kollegen an der Universität Irvine und dem Brookhaven National Laboratory ist es jetzt gelungen, den Aufbau einer Fibrille des für die Krankheit gefährlichsten Beta-Amyloid-Peptids 1–42 mit atomarer Auflösung aufzuklären.
Die Forscher bauten dabei auf Arbeiten der Universität Chicago über die Struktur von Beta-Amyloid Monomeren auf. Weitere immunologische Untersuchungen wiesen nach, dass die untersuchte Form der Fibrillen besonders krankheitsrelevant ist.
Proteinfibrillen sind in elektronenmikroskopischen Aufnahmen zwar sichtbar (Abb. 1), aber es ist sehr schwierig, ins atomare Detail zu gehen. Die dafür gebräuchlichen strukturbiologischen Methoden setzen voraus, dass das Makromolekül entweder als möglichst regelmäßiger Kristall oder in Form einzelner gelöster Moleküle in Wasser vorliegt. Fibrillen sind jedoch langgestreckte Gebilde, die unter sich verkleben und weder Kristalle bilden noch in Wasser gelöst werden können.
Einzig die Festkörper-Kernresonanzspektroskopie (Festkörper-NMR) ist hier in der Lage, Einblick auf atomarer Ebene zu bieten. Neue methodische Entwicklungen erlauben es, ein Netzwerk von Distanzen zwischen Atomen der Proteinmoleküle in einer Fibrille auszumessen (Abb. 2). Daraus konnte in umfangreichen Rechnungen der atomare Aufbau der Fibrille rekonstruiert werden.
Der Hauptteil des Beta-Amyloid 1–42 Peptids nimmt die Struktur eines doppelten Hufeisens an (Abb. 3). Jeweils zwei gleiche Moleküle in einer Ebene bilden, aufeinandergestapelt, eine lange Fibrille. Viele Wasserstoffbrückenbindungen parallel zur Längsachse geben der Fibrille ihre hohe Stabilität.
„Die Struktur unterscheidet sich grundlegend von früheren Modellstudien, für die kaum experimentelle Messdaten zur Verfügung standen“, erklärt Prof. Peter Güntert, Professor für Computergestützte Strukturbiologie an der Goethe-Universität.
In Fachkreisen haben die Publikationen der europäischen und amerikanischen Teams, die einander bestätigen, für Aufsehen gesorgt, denn erstmals ist es möglich, auf Grundlage der Struktur gezielt nach Arzneistoffen zu suchen, die Beta-Amyloid Fibrillen angreifen. Die Forscher hoffen, dass in den nächsten ein bis zwei Dekaden der vor 110 Jahren von dem Frankfurter Arzt Alois Alzheimer erstmals beschriebenen Geißel des Alters der Schrecken genommen werden kann.
Publikationen:
Wälti, M. A., Ravotti, F., Arai, H., Glabe, C., Wall, J., Böckmann, A., Güntert, P., Meier, B. H. & Riek, R. Atomic-resolution structure of a disease-relevant Aβ(1-42) amyloid fibril. Proceedings of the National Academy of Sciences of the United States of America, DOI 10.1073/pnas.1600749113.
http://www.pnas.org/content/early/2016/07/27/1600749113
Colvin, M. T., Silvers, R., Ni, Q. Z., Can, T. V., Sergeyev, I., Rosay, M., Donovan, K. J., Michael, B., Wall, J., Linse, S. & Griffin, R. G. Atomic resolution structure of monomorphic Aβ42 amyloid fibrils. Journal of the American Chemical Society, DOI 10.1021/jacs.6b05129.
Xiao, Y., Ma, B., McElheny, D., Parthasarathy, S., Long, F., Hoshi, M., Nussinov, R. & Ishii, Y. Aβ(1–42) fibril structure illuminates self-recognition and replication of amyloid in Alzheimer’s disease. Nature Structural & Molecular Biology 22, 499–505 (2015).
Bilder zum Download finden sie hier: www.uni-frankfurt.de/62697618
Bildtexte:
Abb. 1: Elektronenmikroskopische Aufnahme der Alzheimer-Fibrillen.
Abb. 2: Netzwerk der Atome im Proteinmolekül
Abb. 3: Struktur der Amyloid-Beta 1–42 Fibrille
Informationen: Prof. Peter Güntert, Institut für Biophysikalische Chemie, Campus Riedberg, Tel.: (069)-798-29621, guentert@em.uni-frankfurt.de.
Die Goethe-Universität ist eine forschungsstarke Hochschule in der europäischen Finanzmetropole Frankfurt. 1914 mit privaten Mitteln überwiegend jüdischer Stifter gegründet, hat sie seitdem Pionierleistungen erbracht auf den Feldern der Sozial-, Gesellschafts- und Wirtschaftswissenschaften, Medizin, Quantenphysik, Hirnforschung und Arbeitsrecht. Am 1. Januar 2008 gewann sie mit der Rückkehr zu ihren historischen Wurzeln als Stiftungsuniversität ein hohes Maß an Selbstverantwortung. Heute ist sie eine der zehn drittmittelstärksten und drei größten Universitäten Deutschlands mit drei Exzellenzclustern in Medizin, Lebenswissenschaften sowie Geistes- und Sozialwissenschaften. Zusammen mit der Technischen Universität Darmstadt und der Universität Mainz ist sie Partner der länderübergreifenden strategischen Universitätsallianz Rhein-Main.
Aktuelle Nachrichten aus Wissenschaft, Lehre und Gesellschaft in GOETHE-UNI online
www.aktuelles.uni-frankfurt.de
Herausgeber: Die Präsidentin
Redaktion: Dr. Anne Hardy, Referentin für Wissenschaftskommunikation, Abteilung PR & Kommunikation, Theodor-W.-Adorno-Platz 1, 60323 Frankfurt am Main, Tel: (069) 798-12498, Fax: (069) 798-763 12531, hardy@pvw.uni-frankfurt.de
Internet: www.uni-frankfurt.de
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Größte bisher bekannte magnetische Anisotropie eines Moleküls gemessen
An der Berliner Synchrotronstrahlungsquelle BESSY II ist es gelungen, die größte magnetische Anisotropie eines einzelnen Moleküls zu bestimmen, die jemals experimentell gemessen wurde. Je größer diese Anisotropie ist, desto besser…

Tsunami-Frühwarnsystem im Indischen Ozean
20 Jahre nach der Tsunami-Katastrophe… Dank des unter Federführung des GFZ von 2005 bis 2008 entwickelten Frühwarnsystems GITEWS ist heute nicht nur der Indische Ozean besser auf solche Naturgefahren vorbereitet….

Resistente Bakterien in der Ostsee
Greifswalder Publikation in npj Clean Water. Ein Forschungsteam des Helmholtz-Instituts für One Health (HIOH) hat die Verbreitung und Eigenschaften von antibiotikaresistenten Bakterien in der Ostsee untersucht. Die Ergebnisse ihrer Arbeit…



