Blutstammzellen machen Hirntumoren aggressiver
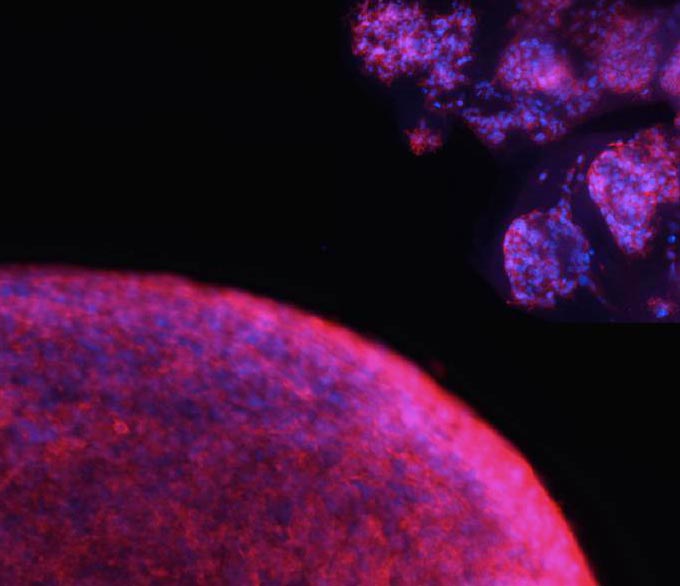
Die Mikroskop-Aufnahme zeigt „Mini-Hirntumoren“, sogenannte Tumor-Organoide, die im Labor aus Zellen von Patienten für die Krebsforschung gezüchtet wurden.
© K. Stratmann und C. Dobersalske
Krebsstudie liefert Ansätze für neue Immuntherapien.
Forschende der Medizinischen Fakultät der Universität Duisburg-Essen haben im Rahmen eines von der Wilhelm Sander-Stiftung geförderten Vorhabens Glioblastome, die aggressivsten Hirntumoren bei Erwachsenen, untersucht und dort erstmals Stammzellen des blutbildenden Systems entdeckt. Das Team des DKTK-Partnerstandorts Essen/Düsseldorf fand heraus, dass diese Blutstammzellen die Teilung der Krebszellen fördern und die Immunabwehr gegen den Tumor unterdrücken. Ihre Entdeckung könnte helfen, wirksamere Immuntherapien gegen die Hirntumoren zu entwickeln. Die Studie wurde in Nature Communications publiziert und in die „Editors‘ Hightlights“ sowie das „Cancer at Nature Portfolio“ aufgenommen.
Glioblastome sind Hirntumoren mit einem besonders schweren und zumeist tödlichen Verlauf. Sie sind selbst mit bestmöglichen chirurgischen, chemo- und strahlentherapeutischen Behandlungen in der Regel nicht langfristig erfolgreich behandelbar. Auch Immuntherapien, die bei anderen Krebsarten bereits gute Erfolge erzielen, schlagen nicht an. Die Ursachen sind bis heute nicht eindeutig geklärt und umso wichtiger ist die Erforschung der zugrundeliegenden Mechanismen.
In einem von der Wilhelm Sander-Stiftung geförderten Forschungsprojekt untersuchte das Team um Krebsforscher Dr. Igor Cima und Prof. Dr. Björn Scheffler, DKTK-Professor für Translationale Onkologie am Westdeutschen Tumorzentrum (WTZ) des Universitätsklinikums Essen (UK Essen), Proben von Glioblastomen und von gesundem Gehirngewebe. Zu ihrer Überraschung entdeckten die Wissenschaftler* in allen Proben von bösartigem Gehirngewebe zum ersten Mal Blutstammzellen und Vorläuferzellen des blutbildenden Systems, die normalerweise im Knochenmark angesiedelt sind. In gesunden Gewebeproben war dieser Zelltyp nicht nachweisbar.
Noch erstaunlicher war ihre Beobachtung, dass diese bislang unbekannten Blutstammzellen offenbar das Immunsystem unterdrücken und zugleich das Tumorwachstum befeuern: „Glioblastome produzieren immunsuppressive Botenstoffe und in der direkten Mikroumgebung der Tumoren finden sich bestimmte Arten von Immunzellen, die die körpereigene Abwehr gezielt drosseln. In unseren Zellkultur-Testsystemen konnten Blutstammzellen die Teilungsaktivität der Krebszellen noch steigern, während die Tumorzellen gleichzeitig die Produktion des als „Immunbremse“ bekannten Moleküls PD-L1 (Programmed cell death 1 ligand 1) auf ihrer Oberfläche erhöhten“, erläutert Björn Scheffler die jetzt entdeckten Zusammenhänge.
Die Forscher untersuchten insgesamt mehrere hundert Gewebeproben von Glioblastom-Patienten. Das Ergebnis: Je mehr Blutstammzellen ein Tumor enthielt, desto mehr immunsuppressive Botenstoffe wurden ausgeschüttet, desto mehr immunbremsende Marker bildeten die Krebszellen – und desto geringer war das Gesamtüberleben der Betroffenen.
Zudem verglich das Team in Kooperation mit Prof. Dr. Ulrich Sure, Direktor der Klinik für Neurochirurgie am UK Essen, gesunde mit kranken Zellen. Durch die Sequenzierung der Genexpression von 660 individuellen Zellen aus vitalem Tumorgewebe konnten Profile erstellt und den Zellen aus gesundem Knochenmark und Blut gegenübergestellt werden. Die Analyse dieser Daten zeigt einige neue Ansätze auf, wie die untersuchte, tumorfördernde Zellpopulation künftig unschädlich gemacht werden könnte.
Dass Blutstammzellen im Knochenmark im Verlauf von Krebserkrankungen bei ihrer Differenzierung bevorzugt zu immunsuppressiven Zelltypen ausreifen, indem sie vom Tumor entsprechend programmiert werden, war der Forschung bereits bekannt. Krebsforscher Igor Cima vermutet ein ähnliches Phänomen jetzt auch bei den Glioblastom-assoziierten Blutstammzellen: „Wir sehen nun erstmals die Möglichkeit, im Rahmen weiterer Forschungsvorhaben modulierend in den Differenzierungsprozess der gliomassoziierten Blutstammzellen einzugreifen – z. B. durch bestimmte Zellbotenstoffe – und auf diese Weise die tumorbedingte Immunblockade zu umgehen. Dann hätten Immuntherapien auch gegen das Glioblastom eine bessere Chance auf Wirksamkeit.“
Die Ergebnisse des Forscherteams wurden jüngst in der renommierten Fachzeitschrift Nature Communications publiziert und zudem in die Editors‘ Hightlights im Fachbereich Focus Cancer und auch in das journalübergreifende Cancer at Nature Portfolio aufgenommen.
Ergänzung zur Abbildung:
Die Mikroskop-Aufnahme zeigt „Mini-Hirntumoren“, sogenannte Tumor-Organoide, die im Labor aus Zellen von Patienten für die Krebsforschung gezüchtet wurden. In Gegenwart von Blutstammzellen vermehren sich Krebszellen in diesen Testsystemen deutlich schneller.
* Die in diesem Text verwendeten Genderbegriffe vertreten alle Geschlechtsformen.
Wilhelm Sander-Stiftung: Partner innovativer Krebsforschung
Die Wilhelm Sander-Stiftung hat das Forschungsprojekt mit rund 191.000 Euro unterstützt.
Stiftungszweck ist die Förderung der medizinischen Forschung, insbesondere von Projekten im Rahmen der Krebsbekämpfung. Seit Gründung der Stiftung wurden insgesamt über 250 Millionen Euro für die Forschungsförderung in Deutschland und der Schweiz ausbezahlt. Damit ist die Wilhelm Sander-Stiftung eine der bedeutendsten privaten Forschungsstiftungen im deutschen Raum. Sie ging aus dem Nachlass des gleichnamigen Unternehmers hervor, der 1973 verstorben ist.
Zum Westdeutschen Tumorzentrum
Am Westdeutschen Tumorzentrum (WTZ) können Patient:innen neben einer bestmöglichen Diagnostik und Therapie zusätzlich davon profitieren, dass erfolgversprechende Ansätze aus der Laborforschung in innovativen klinischen Studien angewandt werden. Das WTZ Zentrum für Neuroonkologie vereint interdisziplinär mehr als 10 Kliniken und Institute der Universitätsmedizin Essen. Ansprechpartner sind Prof. Dr. Ulrich Sure (Direktor der Klinik für Neurochirurgie und Wirbelsäulenchirurgie), Prof. Dr. Martin Glas (Leiter der Abteilung Klinische Neuroonkologie der Klinik für Neurologie) und Prof. Dr. Björn Scheffler (Direktor der DKFZ-Abteilung für Translationale Neuroonkologie am WTZ).
Zum Deutschen Konsortium für Translationale Krebsforschung (DKTK)
Im DKTK verbindet sich das Deutsche Krebsforschungszentrum (DKFZ) in Heidelberg als Kernzentrum langfristig mit onkologisch besonders ausgewiesenen universitären Partnerstandorten in Deutschland. Das DKFZ ist mit mehr als 3.000 Mitarbeiter:innen die größte biomedizinische Forschungseinrichtung in Deutschland. Die Wissenschaftler:innen erforschen, wie Krebs entsteht, erfassen Risikofaktoren und suchen nach neuen Strategien, die verhindern, dass Menschen an Krebs erkranken. Sie entwickeln neue Methoden, mit denen Tumoren präziser diagnostiziert und Betroffene erfolgreicher behandelt werden können.
Kontakt:
Henrike Boden
Wilhelm Sander-Stiftung
Presse- und Öffentlichkeitsarbeit & Stiftungskommunikation
Tel.: +49 (0) 89 544187-0
Fax: +49 (0) 89 544187-20
E-Mail: boden@sanst.de
Martin Rolshoven
Wissenschaftsredaktion
Dekanat der Medizinischen Fakultät der Universität Duisburg-Essen
Hufelandstraße 55
45147 Essen
Tel.: +49 (0)201 723-6274
E-Mail: martin.rolshoven@uk-essen.de
Wissenschaftliche Ansprechpartner:
Dr. rer. nat. Igor Cima
Senior Medical Scientist, DKTK-Neuroonkologie / Immunonkologie
DKFZ-Abteilung für Translationale Neuroonkologie am WTZ
DKTK Partnerstandort Universitätsklinikum Essen
Hufelandstraße 55
45147 Essen
Tel.: +49 (0) 201 723-8141
E-Mail i.cima@dkfz.de
https://www.translationale-neuroonkologie.org/forschung/experimentelle-neuroonko…
Prof. Dr. Björn Scheffler
Direktor der DKFZ-Abteilung für Translationale Neuroonkologie am WTZ
DKTK Partnerstandort Universitätsklinikum Essen
Hufelandstraße 55
45147 Essen
Tel.: +49 (0) 201 723-8131
E-Mail b.scheffler@dkfz-heidelberg.de
https://www.translationale-neuroonkologie.org/uber-uns/uberblick/dktk-neuroonkol…
Originalpublikation:
Lu IN, Dobersalske C, Rauschenbach L, Teuber-Hanselmann S, Steinbach A, Ullrich V, Prasad S, Blau T, Kebir S, Siveke JT, Becker JC, Sure U, Glas M, Scheffler B, Cima I. Tumor-associated hematopoietic stem and progenitor cells positively linked to glioblastoma progression. Nat Commun. 2021 Jun 23;12(1):3895.
DOI: 10.1038/s41467-021-23995-z
Artikel: https://www.nature.com/articles/s41467-021-23995-z
Editors‘ Hightlights: https://www.nature.com/ncomms/editorshighlights
Life sciences research: https://www.nature.com/ncomms/editorshighlights#life
Focus Cancer: https://www.nature.com/collections/aahajfhafc
Cancer at Nature Portfolio: https://www.nature.com/collections/bpwtvhdwgf
Weitere Informationen:
https://www.wilhelm-sander-stiftung.de/
https://www.translationale-neuroonkologie.org/forschung/experimentelle-neuroonko…
https://www.translationale-neuroonkologie.org/uber-uns/uberblick/dktk-neuroonkol…
https://www.uni-due.de/me/meldung.php?id=1217
https://www.dkfz.de/de/presse/pressemitteilungen/2021/dkfz-pm-21-38-Blutstammzel…
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge
Menschen vs Maschinen – Wer ist besser in der Spracherkennung?
Sind Menschen oder Maschinen besser in der Spracherkennung? Eine neue Studie zeigt, dass aktuelle automatische Spracherkennungssysteme (ASR) unter lauten Bedingungen eine bemerkenswerte Genauigkeit erreichen und manchmal sogar die menschliche Leistung…

Nicht in der Übersetzung verloren: KI erhöht Genauigkeit der Gebärdenspracherkennung
Zusätzliche Daten können helfen, subtile Gesten, Handpositionen und Gesichtsausdrücke zu unterscheiden Die Komplexität der Gebärdensprachen Gebärdensprachen wurden von Nationen weltweit entwickelt, um dem lokalen Kommunikationsstil zu entsprechen, und jede Sprache…

Brechen des Eises: Gletscherschmelze verändert arktische Fjordökosysteme
Die Regionen der Arktis sind besonders anfällig für den Klimawandel. Es mangelt jedoch an umfassenden wissenschaftlichen Informationen über die dortigen Umweltveränderungen. Forscher des Helmholtz-Zentrums Hereon haben nun an Fjordsystemen anorganische…



