Das „Selenosom“: Choreografie einer Umprogrammierung
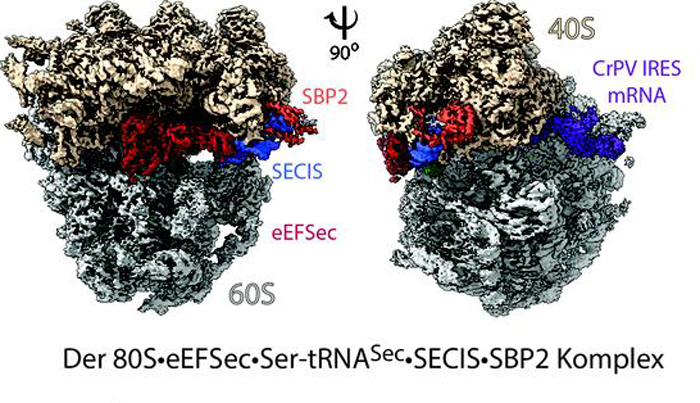
Struktur des „Selenosoms“, dreidimensionale Kryo-EM-Rekonstruktion des ribosomalen Komplexes mit einer Auflösung von 2,8 Ångström.
© Charité | C. M. T. Spahn
Kryo-Elektronenmikroskopie macht zelluläre Strukturen sichtbar.
Einem Team unter Leitung von Forschenden der Charité – Universitätsmedizin Berlin ist es gelungen, einen grundlegenden Vorgang der Molekularbiologie aufzuklären: den Einbau der sogenannten 21. Aminosäure Selenocystein in sogenannte Selenoproteine. Diese besonderen Eiweiß-Konstrukte sind für Säugetiere, Menschen, aber auch einige Mikroorganismen lebensnotwendig. Wie sie im Körper entstehen und zusammengefügt werden, war bislang unbekannt. Im Fachmagazin Science* beschreiben die Autoren erstmals im Detail, wie eine spezielle Bindungstasche im Zusammenspiel mit verschiedenen weiteren Faktoren diesen Vorgang ermöglicht.
Selenoproteine sind eine ungewöhnliche Gruppe von Proteinen, die noch gar nicht so lang bekannt ist. Man geht von bis zu 50 dieser Eiweiße aus, nur ein Teil von ihnen ist bisher erforscht. Sie alle sind komplex aufgebaut und enthalten im Zentrum mindestens einen Teil der namensgebenden Aminosäure Selenocystein (Sec). Selenoproteine übernehmen wichtige Schutz- und Abwehrfunktionen in der Zelle und im menschlichen Körper. Vor allem fungieren sie als sogenannte Oxidoreduktasen, also Vermittler zentraler chemischer Reaktionen, und als Schilddrüsenhormone. Es wird auch vermutet, dass Selenoproteine zum Schutz vor Tumoren beitragen, da sie das Element Selen tragen und oxidativem Stress schnell entgegenwirken können.

© Charité | C. M. T. Spahn
Doch wie kommen diese besonderen Eiweiße zustande? Wie funktioniert die molekulare Choreografie beim Einbau von Selenocystein während des Zusammenfügens der Proteine, der Proteinbiosynthese? Und wie genau sieht die Struktur des „Selenosoms“ aus, jenem Komplex, der sich bildet, um Selenoproteine herzustellen? Das Team um Prof. Dr. Christian Spahn, Direktor des Instituts für Medizinische Physik und Biophysik der Charité, und Dr. Tarek Hilal, Institut für Chemie und Biochemie der Freien Universität Berlin, konnte gemeinsam mit Partnern am Max-Planck-Institut für Molekulare Genetik, an der University of Illinois, Chicago und der Rutgers-Robert Wood Johnson Medical School, New Jersey, mittels hochauflösender, dreidimensionaler Kryo-Elektronenmikroskopie diesen fundamentalen molekularbiologischen Vorgang strukturell und mechanistisch nachvollziehen.
Ribosomen, die Proteinfabriken der Zelle, stellen Proteine normalerweise streng nach den von den messenger RNAs (mRNAs) gelieferten Bauplänen her. Der universelle genetische Code definiert anhand bestimmter Sequenzen, bestehend aus jeweils drei variierenden Basen, den mRNA-Triplett-Codons, welche Aminosäure an welcher Stelle eines Proteins eingebaut wird. Selenoproteine haben allerdings einen speziellen Aufbau, sodass die 20 Standardaminosäuren bei ihnen nicht ausreichen. Sie enthalten an bestimmten Stellen die sogenannte 21. Aminosäure, das Selenocystein (Sec).
Da für den Einbau von Selenocystein kein eigenes Codon, also keine verschlüsselnde Basensequenz existiert, entsteht beim Bau von Selenoproteinen im ribosomalen Komplex eine grundlegende Besonderheit. Durch eine gesonderte Signalsequenz in der mRNA, das sogenannte SECIS-Element (Selenocystein-Insertionssequenz), wird das Ribosom umprogrammiert und die genetische Information quasi überschrieben. Ein Codon, das normalerweise einen Kettenabbruch und damit die Fertigstellung des Proteins programmiert (UGA-Stopcodon), wird an den gewünschten Stellen zu einem neuen Codon, und zwar dem Codon zum Einbau von Selenocystein. Dieser Rekodierungsvorgang erfordert neben dem SECIS-Element zusätzlich eine besondere, mit Selenocystein beladene Transfer-RNA (tRNASec) und zusätzliche, spezialisierte Translationsfaktoren. „Zwar sind die beteiligten Player seit einigen Jahren bekannt, dennoch blieb bislang ein Rätsel, wie sie genau funktionieren und wie sie zusammenwirken“, so Prof. Spahn. „Vor allem, wie im Einzelnen das SECIS-Element wirkt, war mysteriös, denn es befindet sich in der linearen Sequenz der mRNA nicht in direkter Nachbarschaft zum umprogrammierten UGA-Stopcodon, sondern am Ende, viele hundert Nukleotid-Bausteine entfernt.“
Um den molekularen Mechanismus aufzuklären, hat das Forschungsteam den ribosomalen Komplex, der sich bildet, um das UGA-Stopcodon zu rekodieren, das „Selenosom“, im Labor nachempfunden. Das hochauflösende Bildgebungsverfahren der Kryo-Elektronenmikroskopie ermöglicht eine dreidimensionale Darstellung des winzigen Konstrukts und somit strukturelle Untersuchungen. „Anhand der abgebildeten Strukturen konnten wir aufklären, wie die beteiligten Faktoren mit dem Ribosom interagieren und wie sie genau zusammenwirken, um das Ribosom umzuprogrammieren“, erklärt Prof. Spahn. „Wir konnten insbesondere zeigen, dass die mRNA eine große Schleife bildet, sodass das UGA-Stopcodon und das SECIS-Element gleichzeitig am Ribosom gebunden sind. Das SECIS-Element wird dabei in einer bislang unbekannten Bindetasche am Ribosom verankert und kann dann, im Ribosomen-gebundenen Zustand, unterstützt durch Translationsfaktoren den Selenocystein-Einbau begünstigen.“ Diese Struktur und die Funktionsweise des „Selenosoms“ haben das Forschungsteam überrascht und waren so nicht vorherzusehen. Denn der Vorgang verläuft bei Säugetieren und beim Menschen deutlich anders als der Einbau von Selenocystein in Bakterien, der zuvor schon bekannt war. Der nun beschriebene Komplex zeigt beispielhaft, wie Signalstrukturen am hinteren Ende einer mRNA, also außerhalb des kodierenden Bereiches, mit dem Ribosom interagieren können, um dieses zu regulieren.
Den ersten Schritt beim Einbau von Selenocystein konnten die Forschenden somit aufklären. Die nachfolgenden Schritte sind noch immer unklar und sollen in weiteren Arbeiten strukturell untersucht werden. Studien wie diese tragen dazu bei, Funktion und Bedeutung des lebenswichtigen Spurenelements Selen in der normalen Physiologie und beim Entstehen von Krankheiten wie Diabetes oder Krebs besser zu verstehen. Die Arbeiten wurden ermöglicht durch die Deutsche Forschungsgemeinschaft (SFB740 und FOR1805) sowie Zuwendungen der Deutschen Forschungsgemeinschaft und des Landes Berlin im für Großgeräte entsprechenden Artikel 91b GG.
Wissenschaftliche Ansprechpartner:
Prof. Dr. Christian Spahn
Direktor des Instituts für Medizinische Physik und Biophysik
Charité – Universitätsmedizin Berlin
t: +49 30 450 524 131
e: christian.spahn@charite.de
Originalpublikation:
https://www.science.org/doi/10.1126/science.abg3875
Weitere Informationen:
https://biophysik.charite.de/ Institut für Medizinische Physik und Biophysik
https://biophysik.charite.de/forschung/ag_kryo_elektronenmikroskopie/ AG Kryo-Elektronenmikroskopie makromolekularer Maschinen
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Sensoren für „Ladezustand“ biologischer Zellen
Ein Team um den Pflanzenbiotechnologen Prof. Dr. Markus Schwarzländer von der Universität Münster und den Biochemiker Prof. Dr. Bruce Morgan von der Universität des Saarlandes hat Biosensoren entwickelt, mit denen…

Organoide, Innovation und Hoffnung
Transformation der Therapie von Bauchspeicheldrüsenkrebs. Bauchspeicheldrüsenkrebs (Pankreaskarzinom) bleibt eine der schwierigsten Krebsarten, die es zu behandeln gilt, was weltweite Bemühungen zur Erforschung neuer therapeutischer Ansätze anspornt. Eine solche bahnbrechende Initiative…

Leuchtende Zellkerne geben Schlüsselgene preis
Bonner Forscher zeigen, wie Gene, die für Krankheiten relevant sind, leichter identifiziert werden können. Die Identifizierung von Genen, die an der Entstehung von Krankheiten beteiligt sind, ist eine der großen…



