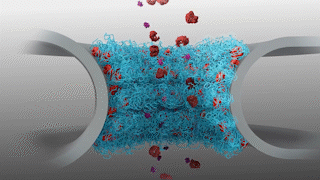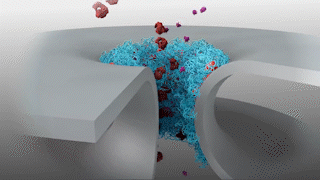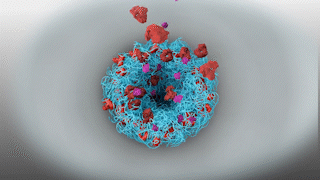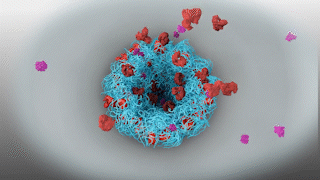
Der Zellkern wird von einer hochgradig gesicherten Tür, der sogenannten Kernpore, bewacht, die den Stofftransport vom Zytoplasma zum Zellkern und zurück regelt. Eine Forschungsgruppe der Universität Basel hat nun gezeigt, dass verschiedene spezialisierte Proteine die Kernpore bewachen, um den unerwünschten Austritt von Stoffen zu verhindern. Dabei bilden diese verschiedenen sogenannten Shuttle-Proteine einen austrittssicheren Mechanismus, indem sie gegenseitig füreinander einspringen und so die Pore absichern.
Die Kernpore ist dafür verantwortlich, den Transport von Proteinen aus dem Zytoplasma in den Zellkern zu regulieren und RNA aus diesem hinauszubefördern. Sie funktioniert dabei wie ein molekulares Sieb, das den Ein- und Austritt von frachttragenden Shuttle-Proteinen kontrolliert. Die Kernpore interagiert dabei mit den Shuttle-Proteinen, die wie Türsteher entscheiden, welche Proteine eintreten dürfen und welche nicht.
Prof. Dr. Roderick Lim vom Biozentrum der Universität Basel erforscht dieses rätselhafte selektive Transportsystem seit mehreren Jahren. Sein Team hat nun in Zusammenarbeit mit dem Swiss Nanoscience Institute drei Shuttle-Proteine in menschlichen Zellen untersucht und herausgefunden, dass ihre Ansammlung an der Kernpore wichtig ist, um den unterwünschten Austritt von Substanzen aus dem Zellkern zu verhindern.
Die Menge der Shuttle-Proteine an der Pore hängt von ihrer Konzentration in der Zelle ab. Wenn sich die Anzahl eines der Shuttle-Protein verringert, können die beiden anderen Shuttle-Proteine deren Platz einnehmen, um die Pore zu verstärken. Die Ergebnisse dieses neuartigen Kompensationsmechanismus wurden nun im «Journal of Cell Biology» veröffentlicht.
Austauschbare Shuttle-Proteine sichern die Kernpore
«Es zeigt sich, dass sich die Shuttle-Proteine, obwohl sie aus der gleichen Rezeptorfamilie stammen, im Hinblick auf ihre Funktion, Fracht, Lokalisierung und Konzentration unterscheiden», sagt Molekularbiologin Dr. Joanna Kalita, Erstautorin der Studie. Die Shuttle-Proteine, die als Schutzgarde an der Kernpore fungieren und darüber entscheiden, welche Fracht in den Zellkern hinein darf und welche hinausbefördert werden muss, befinden sich – abhängig von ihrer jeweiligen Konzentration – in unterschiedlicher Menge in der Kernpore.
Veränderten die Forscher die Konzentration eines der Shuttle-Proteine, änderte sich auch die Anzahl der anderen beiden Proteine, die die Kernpore besetzten. «Wenn die Gesamtzahl der Shuttle-Proteine in der Pore reduziert wird, wird die Kernpore undicht. Zellen verlassen sich also auf einen Mechanismus, der es ermöglicht, den Verlust eines Shuttle-Proteins durch die Zunahme und den Einsatz eines der anderen auszugleichen. So sichern die Shuttle-Proteine die Kernporen», sagt Kalita.
Erkrankungen durch defekte Kernporen
Schäden an diesem biologischen Sicherheitssystem sind schädlich für Zellen und stehen mit Krebs und neurodegenerativen Erkrankungen in Verbindung. Viren, die Zellen infizieren, wie etwa SARS-CoV-2, können diese Shuttle-Proteine auch von der Kernpore fernhalten, um ihre Funktionalität zu beeinträchtigen. «Das kann zu Defekten in der Kernpore führen und in der Folge können unerwünschte Stoffe ungehindert in die Kernporen eindringen und den Zellkern quasi vergiften.
Umgekehrt können für den Zellkern wichtige Stoffe nicht mehr eingeführt werden. Und somit sind ein besseres Verständnis in die Funktion der Kernpore wichtig, um die Ursachen und Folgen eines fehlerhaften Transports im Hinblick auf Krankheiten zu verstehen», erklärt Lim.
Originalpublikation
Joanna Kalita, Larisa E. Kapinos, Tiantian Zheng, Chantal Rencurel, Anton Zilman und Roderick Y. H. Lim
Karyopherin enrichment and compensation fortifies the nuclear pore complex against nucleocytoplasmic leakage.
Journal of Cell Biology (2022), doi: 10.1083/jcb.202108107
Weitere Informationen:
https://www.unibas.ch/de/Aktuell/News/Uni-Research/Schutzgarde-fuer-den-Zellkern.html