Schutzimpfung gegen veränderte Proteine könnte Krebsentstehung verhindern
© DKFZ
Krebsarten, bei denen ein Defekt der Erbgut-Reparatur vorliegt, zeichnen sich durch eine besonders hohe Zahl an Mutationen aus. Wissenschaftlern des Deutschen Krebsforschungszentrums (DKFZ), des Universitätsklinikums Heidelberg, der Universität Heidelberg und des Heidelberger Instituts für Theoretische Studien (HITS) ist es nun gelungen, bei diesen Tumoren solche Mutationen zu identifizieren, die in identischer Form bei zahlreichen Patienten übereinstimmen und die darüber hinaus zu veränderten Proteinstrukturen führen. Impfungen gegen diese veränderten Proteine könnten zukünftig die Entstehung dieser Krebsformen im Keim ersticken, wenn sie sich in klinischen Studien bewähren.
Erbgutveränderungen führen häufig dazu, dass Zellen veränderte Proteine ausbilden. Besonders häufig tritt dies bei den so genannten Mikrosatelliten-instabilen Krebsarten auf: In diesen Tumoren ist ein wichtiges Reparatursystem ausgefallen, das normalerweise kleine Fehler im Erbgut korrigiert. Bleiben solche DNA-Defekte unrepariert, so schiebt sich häufig ein zusätzlicher Baustein in die DNA-Kette ein – mit der Folge, dass die gesamte Proteinbauanleitung aus dem Takt gerät.
Die dadurch entstehenden neuartigen Proteinstrukturen, so genannte Neoantigene, werden vom Immunsystem oft als fremd erkannt. „Bekanntermaßen sprechen Tumoren mit DNA-Reparaturdefekten, die viele Neoantigene haben, auch besonders gut auf Immuntherapien an“, erklärt der Leiter der Studie Matthias Kloor vom Universitätsklinikum Heidelberg und vom Deutschen Krebsforschungszentrum.
Etwa 15 Prozent aller Fälle von Darmkrebs und bis zu 30 Prozent aller Gebärmutterkörper-Karzinome zählen zu den Mikrosatelliten-instabilen Tumoren. Bislang war nicht bekannt, ob diese Neoantigene bei Mikrosatelliten-instabilen Krebsarten nach dem Zufallsprinzip entstehen oder ob es bestimmte Häufigkeiten gibt.
Um das herauszufinden, unterzogen Kloor und sein Team daher nun 139 Mikrosatelliten-instabile Tumoren einer systematischen Analyse. Dazu nutzen die Forscher einen neu am Universitätsklinikum, am DKFZ, am Interdisziplinären Zentrum für Wissenschaftliches Rechnen der Universität Heidelberg und am HITS entwickelten Algorithmus, der die Mutationen in den Tumorzellen quantitativ auswertet. In einem zweiten Schritt konnten die Wissenschaftler vorhersagen, welche dieser Neoantigene dazu fähig sind, das Immunsystem zu aktivieren.
Das überraschende Ergebnis der Untersuchung: Die Mutationen treten keineswegs rein zufällig an beliebigen Stellen des Erbguts auf. Vielmehr fanden die Wissenschaftler zahlreiche spezifische wiederkehrende Erbgutveränderungen, die in den Tumoren vieler Patienten übereinstimmten. Viele dieser übereinstimmenden Mutationen führen zur Bildung von Neoantigenen, die laut bioinformatischer Vorhersage in der Lage sind, das Immunsystem zu aktivieren und damit gegen den Krebs zu mobilisieren.
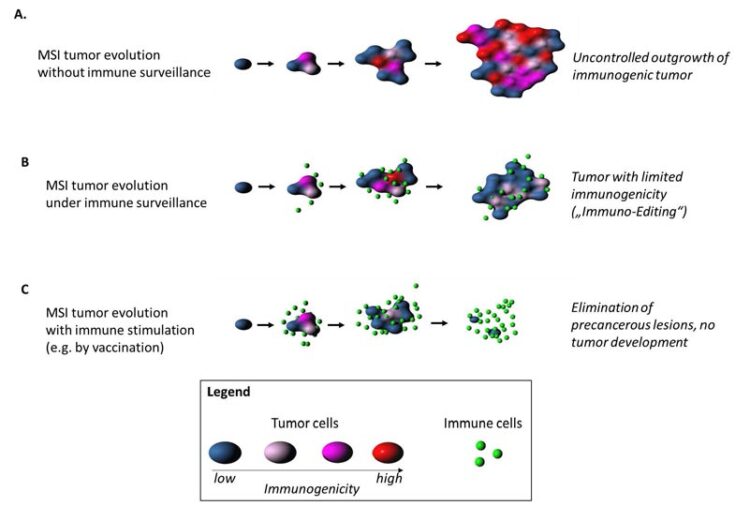
Die zweite Überraschung: Mutationen, die zu stark immunogenen Neoantigenen führen, finden sich bei den Mikrosatelliten-instabilen (MSI) Krebsarten tatsächlich eher selten. „Das kann darauf hinweisen, dass das Immunsystem den Tumor während seiner Entstehung überwacht und Krebszellen mit hoch immunogenen Neoantigenen sogleich eliminiert. Der Tumor besteht dann mehrheitlich aus Zellen, deren Neoantigene das Immunsystem deutlich weniger aktivieren. Das Immunsystem formt also den Tumor im Verlaufe seiner Entstehung“, erklärt Matthias Kloor. Jedoch gibt es bestimmte Mutationen, die trotz der hohen Immunogenität der entstehenden Neoantigene häufig in MSI-Tumoren vorkommen. Diese Mutationen scheinen die Tumor-Entstehung voranzutreiben. Solche Neoantigene, die von Mutationen mit Tumor-treibendem Effekt resultieren, sind für eine Impfstoffentwicklung besonders vielversprechend.
„Diese Beobachtung bestätigt unsere Idee, dass es möglich sein könnte, mit Schutzimpfungen gegen ausgewählte Neoantigene die Entstehung klinisch relevanter Tumoren zu verhindern“, sagt Magnus von Knebel Doeberitz, ebenfalls Autor der Arbeit und Leiter einer sowohl am DKFZ als auch am Universitätsklinikum Heidelberg angesiedelten Forschungsabteilung.
Besonders profitieren könnten davon Patienten mit Lynch-Syndrom, bei denen Defekte der DNA-Reparatur familiär auftreten und die daher häufig schon in jüngerem Alter an Krebs erkranken. Die Idee der Forscher ist, das Immunsystem dieser Patienten spezifisch für solche Neoantigene zu sensibilisieren, die aus Mutationen resultieren, die das bösartige Krebswachstum besonders antreiben. Damit könnte die Tumorentwicklung so beeinflusst werden, dass das Auswachsen von gefährlichen Krebszellklonen deutlich weniger wahrscheinlich wird. Vor einer klinischen Anwendung ist es jedoch erforderlich, diesen präventiven Ansatz in weiteren vorklinischen und klinischen Studien auf seine Wirksamkeit zu untersuchen.
Originalpublikation:
Alexej Ballhausen, Moritz Jakob Przybilla, Michael Jendrusch, Saskia Haupt, Elisabeth Pfaffendorf, Markus Draxlbauer, Florian Seidler, Sonja Krausert, Aysel Ahadova, Martin Simon Kalteis, Daniel Heid, Damian Stichel, Johannes Gebert, Maria Bonsack, Sarah Schott, Hendrik Bläker, Toni Seppälä, Jukka-Pekka Mecklin, Sanne Ten Broeke, Maartje Nielsen, Vincent Heuveline, Julia Krzykalla, Axel Benner, Angelika Beate Riemer, Magnus von Knebel Doeberitz, Matthias Kloor: The shared neoantigen landscape of MSI cancers suggests immunoediting during tumor evolution
Nature Communications 2020, DOI: 10.1038/s41467-020-18514-5.
Das Deutsche Krebsforschungszentrum (DKFZ) ist mit mehr als 3.000 Mitarbeiterinnen und Mitarbeitern die größte biomedizinische Forschungseinrichtung in Deutschland. Über 1.300 Wissenschaftlerinnen und Wissenschaftler erforschen im DKFZ, wie Krebs entsteht, erfassen Krebsrisikofaktoren und suchen nach neuen Strategien, die verhindern, dass Menschen an Krebs erkranken. Sie entwickeln neue Methoden, mit denen Tumoren präziser diagnostiziert und Krebspatienten erfolgreicher behandelt werden können.
Beim Krebsinformationsdienst (KID) des DKFZ erhalten Betroffene, interessierte Bürger und Fachkreise individuelle Antworten auf alle Fragen zum Thema Krebs.
Gemeinsam mit Partnern aus den Universitätskliniken betreibt das DKFZ das Nationale Centrum für Tumorerkrankungen (NCT) an den Standorten Heidelberg und Dresden, in Heidelberg außerdem das Hopp-Kindertumorzentrum KiTZ. Im Deutschen Konsortium für Translationale Krebsforschung (DKTK), einem der sechs Deutschen Zentren für Gesundheitsforschung, unterhält das DKFZ Translationszentren an sieben universitären Partnerstandorten.
Die Verbindung von exzellenter Hochschulmedizin mit der hochkarätigen Forschung eines Helmholtz-Zentrums an den NCT- und den DKTK-Standorten ist ein wichtiger Beitrag, um vielversprechende Ansätze aus der Krebsforschung in die Klinik zu übertragen und so die Chancen von Krebspatienten zu verbessern.
Das DKFZ wird zu 90 Prozent vom Bundesministerium für Bildung und Forschung und zu 10 Prozent vom Land Baden-Württemberg finanziert und ist Mitglied in der Helmholtz-Gemeinschaft Deutscher Forschungszentren.
Ansprechpartner für die Presse:
Dr. Sibylle Kohlstädt
Pressesprecherin
Strategische Kommunikation und Öffentlichkeitsarbeit
Deutsches Krebsforschungszentrum
Im Neuenheimer Feld 280
69120 Heidelberg
T: +49 6221 42 2843
F: +49 6221 42 2968
E-Mail: S.Kohlstaedt@dkfz.de
E-Mail: presse@dkfz.de
www.dkfz.de
Media Contact
Alle Nachrichten aus der Kategorie: Medizin Gesundheit
Dieser Fachbereich fasst die Vielzahl der medizinischen Fachrichtungen aus dem Bereich der Humanmedizin zusammen.
Unter anderem finden Sie hier Berichte aus den Teilbereichen: Anästhesiologie, Anatomie, Chirurgie, Humangenetik, Hygiene und Umweltmedizin, Innere Medizin, Neurologie, Pharmakologie, Physiologie, Urologie oder Zahnmedizin.
Neueste Beiträge

Sensoren für „Ladezustand“ biologischer Zellen
Ein Team um den Pflanzenbiotechnologen Prof. Dr. Markus Schwarzländer von der Universität Münster und den Biochemiker Prof. Dr. Bruce Morgan von der Universität des Saarlandes hat Biosensoren entwickelt, mit denen…

Organoide, Innovation und Hoffnung
Transformation der Therapie von Bauchspeicheldrüsenkrebs. Bauchspeicheldrüsenkrebs (Pankreaskarzinom) bleibt eine der schwierigsten Krebsarten, die es zu behandeln gilt, was weltweite Bemühungen zur Erforschung neuer therapeutischer Ansätze anspornt. Eine solche bahnbrechende Initiative…

Leuchtende Zellkerne geben Schlüsselgene preis
Bonner Forscher zeigen, wie Gene, die für Krankheiten relevant sind, leichter identifiziert werden können. Die Identifizierung von Genen, die an der Entstehung von Krankheiten beteiligt sind, ist eine der großen…



